合成生物学是一门新兴的交叉学科,通过结合多学科理论和方法,设计并构建生物分子和生物系统,实现生物体系的定制化和优化,已经在多个领域展现了广阔的应用前景和革命性的潜力。我校生命与环境科学学院杨林教授团队长期致力于岩白菜素的合成生物学研究,4月26日研究成果以“unravelling and reconstructing the biosynthetic pathway of bergenin”为题在线发表于国际重要学术期刊——nature子刊《nature communications》(if=16.6)上。论文链接:。

图1. 文章在线发表截图
岩白菜素(bergenin, 1)为没食子酸c-糖苷类化合物,具有镇咳祛痰等多种药理活性,临床上用于治疗慢性气管炎等呼吸道疾病,需求量大。由于野生植物资源匮乏,化学合成困难,导致药源不足,开展其合成生物学研究可为解决该问题提供新策略,具有重要意义。
目前,岩白菜素的生物合成途径尚未完全解析,尤其是没食子酸后修饰关键酶2-c-糖基转移酶(2-c‑glycosyltransferase, 2-cgt)与4-o-甲基转移酶(4-o-methyltransferase, 4-omt)及其催化反应顺序未被揭示,是其生物合成研究的难点,阐明岩白菜素生物合成途径中没食子酸后修饰关键酶cgt(s)和omt(s)至关重要。在此基础上,通过模块化方式,在大肠杆菌中重构和优化岩白菜素前体4-o-甲基没食子酸2-c-b-d-葡萄糖苷(4-o-methyl gallic acid 2-c-β-d-glycoside, 4-omga-glc, 4)从头生物合成途径,并通过化学法酯化合成岩白菜素(图2),实现岩白菜素的规模化生产,为岩白菜素的获取提供了全新方案,有望解决其临床用药来源问题。
图2. 在大肠杆菌中由葡萄糖起始从头人工合成岩白菜素的设计方案
第一,首先解析了岩白菜素的生物合成途径。从含有岩白菜素的药用植物紫金牛(ardisia japonica)中发掘出催化活性较高的岩白菜素生物合成途径中的关键酶2-c-糖基转移酶ajcgt1和4-o-甲基转移酶ajomt2(图3),能分别催化各自假设前体形成对应的2-c-糖基化产物、4-o-甲基化产物。酶动力学的研究结果表明,没食子酸在ajomt2的催化下形成4-o-甲基没食子酸,在ajcgt1的催化下形成4-omga-glc。
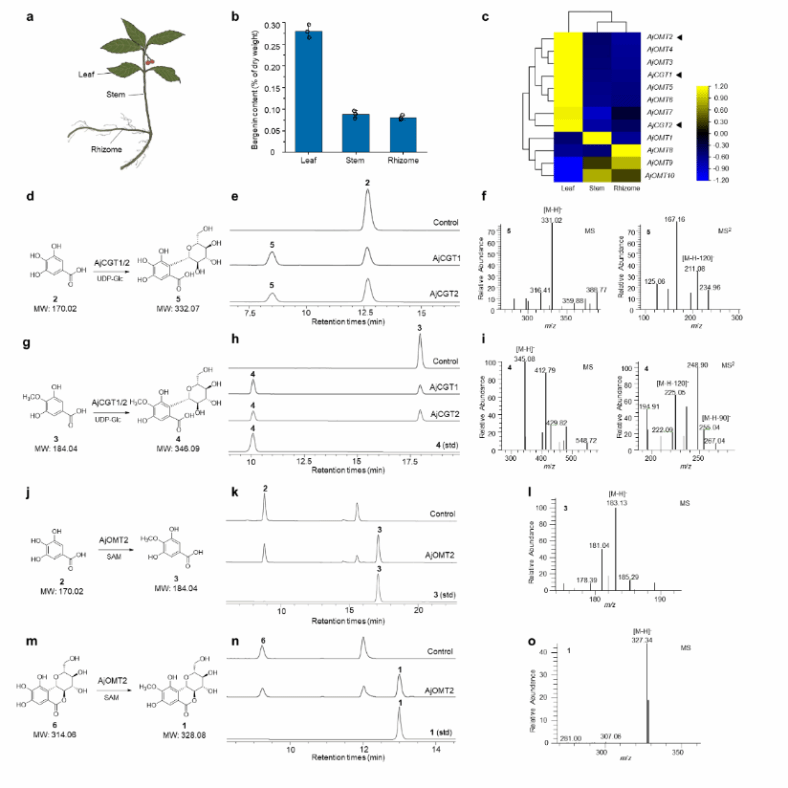
图3.岩白菜素生物合成途径中的2-cgts和4-omts的功能鉴定
第二,从头生物合成岩白菜素前体4-omga-glc。将ajcgt1和ajomt2的基因共表达到e. colibl21 (de3)菌株,得到三个工程菌e1-e3,均能催化外源底物没食子酸(2)生成岩白菜素的前体4-omga-glc,成功构建了omt-cgt模块。通过在e. coli bl21 (de3)菌株中引入来自铜绿假单胞菌(pseudomonas fluorescens)羟化酶突变体poba**基因,过表达内源分支酸裂解酶ubic基因,构建工程菌s1−s3。三种工程菌均能生产没食子酸,其中工程菌s1没食子酸的产量达到619mg/l,成功构建没食子酸生产模块。
将ajomt2-ajcgt1的基因引入到生产没食子酸(2)的菌株中,得到工程菌a1−a6(图4)。6种菌株培养液中均检测到4-omga-glc。其中工程菌a3的4-omga-glc产量最高,诱导表达48 h产量达418.13 mg/l。菌株a1–a6均可以利用葡萄糖生产4-omga-glc,从而重构了4-omga-glc (4)的从头生物合成途径。
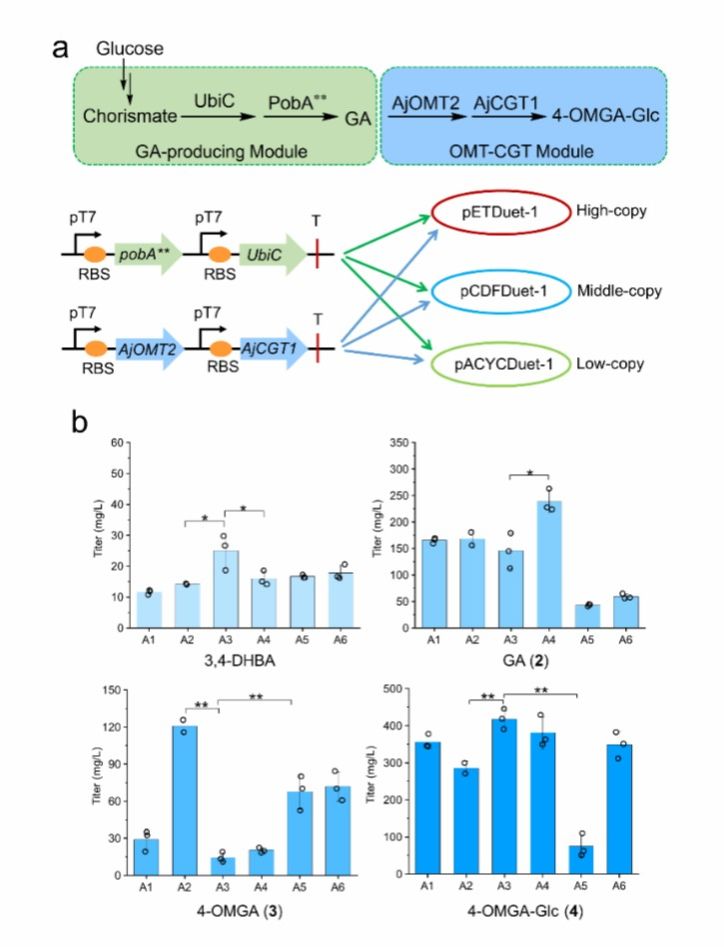
图4.在e. coli中以葡萄糖为碳源从头合成岩白菜素前体4-omga-glc (4)
第三,优化白菜素前体4-omga-glc的生物合成途径。采用半理性设计方法,优化ajomt2和ajcgt1的催化活性。ajomt2突变体ajomt2-y203t(命名为ajomt2*)对没食子酸的催化效率提高1.3倍;ajcgt1突变体ajcgt1-a332f(命名为ajcgt1*)对没食子酸的转化率提高1.4倍(图5)。携带ajomt2-ajcgt1*或ajomt2*-ajcgt1的工程菌均能显著提高对没食子酸的转化效率。密码子优化是提高酶催化效率另一有效途径。携带有密码子优化的ajomt2-y203t (即ajomt2*opt)和ajcgt1(即ajcgt1opt)基因的工程菌株y4对没食子酸(2)的催化效率提升了2.3倍(图5)。将密码子优化后的上述两个基因引入到生产没食子酸的底盘细胞中,获得工程菌d1在摇瓶培养条件下,4-omga-glc产量在48 h达到560.1 mg/l。
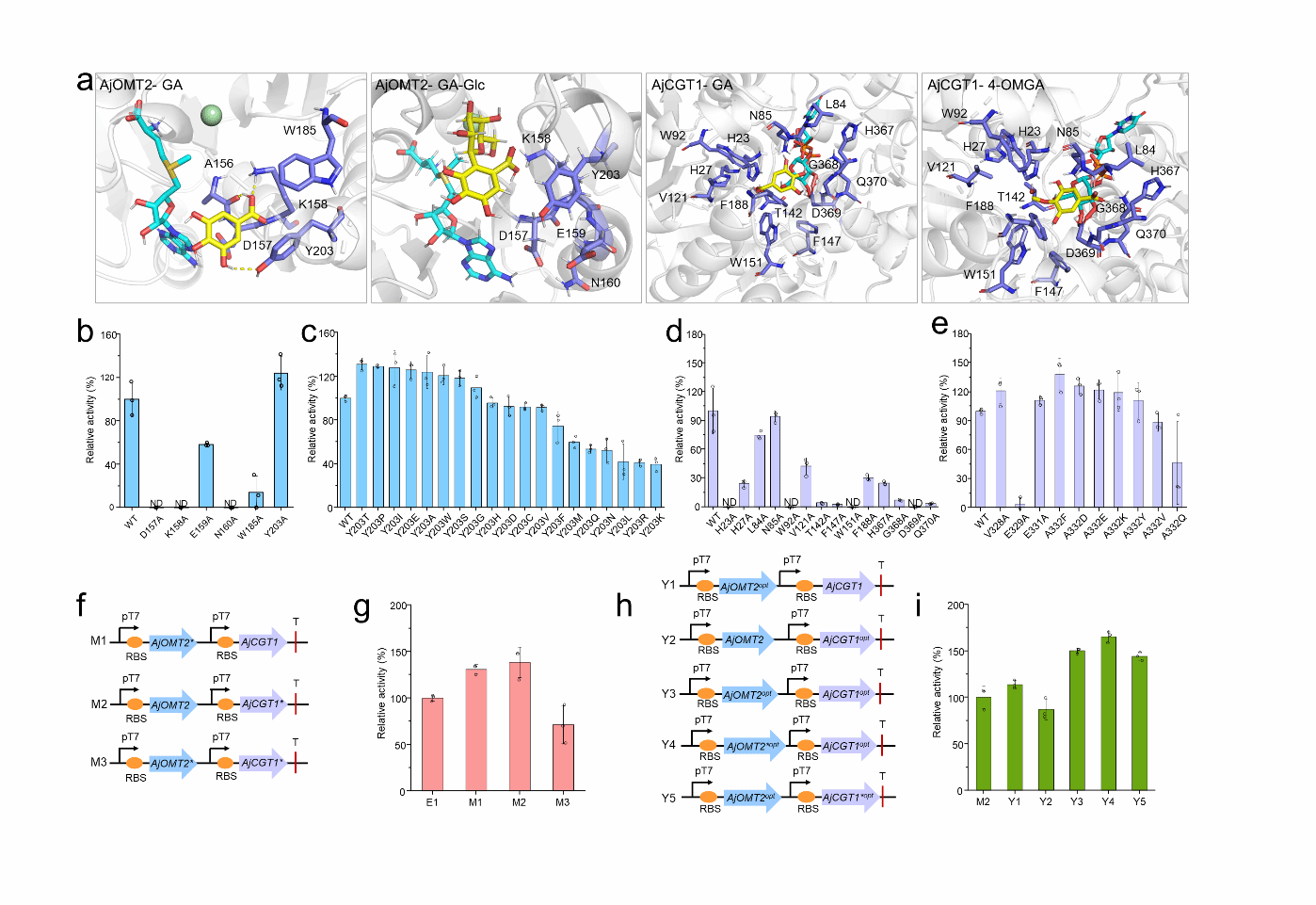
图5.通过半理性设计和密码子优化提高omt-cgt模块的催化效率
进一步优化供体供应模块。甲基供体sam和糖基供体udp-glc是岩白菜素生物合成途径中的重要供体。过表达sam再生循环中关键基因mtn和luxs,有效提升4-omga-glc的产量。供体模块的优化后的高产菌株d4在摇瓶发酵培养条件下,48 h目标产物4-omga-glc的产量在达到609.5 mg/l。工程菌d4在3 l生物反应器中产生的4-omga-glc产量达到1.49 g/l,酸化后岩白菜素的理论产量达到1.41 g/l。
本研究的创新点在于通过对岩白菜素生物合成途径关键酶的发掘及功能鉴定,首次解析岩白菜素的完整生物合成途径;重构和优化岩白菜素从头生物合成途径,实现岩白菜素的规模化生产。本研究为岩白菜素的获取提供全新方案,有望解决其临床用药来源问题。
中央民族大学生物学硕士生闫锐琪(2020级硕士生)、谢冰寒(2021级硕士生)、刘琦(2019级硕士生)为该论文共同第一作者,2017级硕士生隋颂扬和2022级硕士生王姝琪为主要参与人,中央民族大学杨林教授和中国医学科学院药物研究所的解可波研究员、戴均贵研究员为共同通讯作者。该项研究工作得到国家自然科学基金(82373995)的资助。
(供稿 杨林 审校 张严 陈坦 王乔)
